INTRODUZIONE
La resistenza agli antibiotici è diventata un vero e proprio problema di sanità pubblica1. La grande disponibilità di nuovi farmaci antibiotici a partire dalla fine degli anni 80 fino all’inizio degli anni 2000 ha permesso l’utilizzo di armi sempre più efficaci per combattere diversi tipi di infezioni, a prezzo tuttavia di aumentare parallelamente la pressione antibiotica sulla popolazione batterica fino a livelli oggi molto critici. Attualmente numerose famiglie e specie batteriche presentano ceppi resistenti anche a nuove classi di antibiotici, dagli MRSA, agli enterobatteri produttori di beta-lattamasi a spettro esteso (ESBL+), fino ad arrivare a situazioni di estrema criticità quali le enterobatteriacee produttrici di carbapenemasi (in modo particolare Klebsiella, KPC). Per trattare le infezioni invasive causate da germi multiresistenti (MDR), si sono recuperati “vecchi” antibiotici, anche con modesta attività e/o significativo grado di tossicità (come la colistina), che tuttavia rappresentano le uniche possibilità terapeutiche in associazione ad altri farmaci. Da oltre vent’anni la ricerca in ambito antibiotico ha prodotto una quantità di molecole sempre minore e all’orizzonte non si intravedono importanti novità2; ciò soprattutto per motivi di tipo economico, in quanto dal punto di vista del mercato è più remunerativo investire in altri settori, specialmente quelli delle malattie croniche. Diventa pertanto impellente la necessità di attuare politiche volte a migliorare ed ottimizzare l’utilizzo della terapia antibiotica: i cosiddetti programmi di antibiotic stewardship, per usare l’espressione anglosassone che designa oggi, nella letteratura medica, il complesso di azioni da mettere in campo per utilizzare al meglio gli antibiotici e prevenire le resistenze. Numerosi lavori sono stati pubblicati in merito a progetti di stewardship condotti in campo ospedaliero3-5, ove il problema è particolarmente sentito sia per motivi di difficile controllo epidemiologico e di esposizione a pratiche invasive, sia per motivi clinici (prevalenza di infezioni invasive in unità intensivistiche, infettivologiche, internistiche, riabilitative). Sono invece pochissime le esperienze pubblicate nell’ambito delle Cure Primarie, nonostante il fatto che la quantità di antibiotici prescritta sul territorio sia quattro volte maggiore rispetto a quella prescritta negli ospedali e conseguentemente il miglioramento prescrittivo potrebbe essere almeno altrettanto strategico6, 7. È noto che una certa quota di prescrizioni in ambito territoriale può essere indotta dalle proposte o prescrizioni specialistiche8,9, ma buona parte viene decisa su iniziativa diretta del Medico di Medicina Generale (MMG). I dati di letteratura a disposizione relativi all’ambito territoriale sono essenzialmente riferiti a interventi in strutture residenziali per anziani, nelle quali la presenza di persone fragili e/o con multimorbidità facilita la possibilità di colonizzazione con germi difficili o MDR10-12. Come detto, si trovano invece pochissime esperienze riferibili direttamente all’ambito della medicina generale13-15, e alcune, peraltro molto interessanti, riguardano non veri e propri progetti di stewardship bensì interventi mirati in generale al contenimento dell’uso di antibiotici16. Abbiamo ritenuto che la nostra esperienza, condotta in un distretto dell’AUSL di Reggio Emilia, e in particolare nel Dipartimento Cure Primarie di Scandiano, potesse essere di interesse sia per questo motivo, sia in quanto nata direttamente dai clinici e quindi più facilmente esportabile anche in altre realtà, del nostro territorio come di altre Aziende sanitarie.
Materiali e Metodi
Presso l’AUSL di Reggio Emilia sono attivi dei “tavoli” permanenti di discussione (cd. Board Distrettuali) composti da rappresentanti della Direzione Sanitaria e di Distretto, dai coordinatori dei Nuclei di Cure Primarie (NCP), dai Direttori delle Unità Operative dell’Ospedale di distretto, dal Dipartimento Farmaceutico e dai Responsabili Infermieristici di Dipartimento. Nel Board ci si confronta sulle modalità di collaborazione e si analizzano in modo integrato i dati relativi alle attività territoriali, specialistiche e alle prescrizioni farmacologiche, con un’attenzione non limitata ai costi ma estesa quando possibile ad altri parametri che configurano l’appropriatezza prescrittiva (“la cosa giusta nel momento e nel modo giusto”). Nei primi mesi del 2014, all’interno del Board si è discusso della prescrizione dei Fluorochinolonici (FC), farmaci per i quali sono segnalati livelli di resistenza ormai molto alti in tutto il mondo17. I Bollettini epidemiologici dell’Agenzia Sanitaria Sociale Regionale e dei Laboratori di Microbiologia aziendali riportano anche nella nostra provincia elevati livelli di resistenza18.
[caption id="attachment_5617" align="aligncenter" width="754"]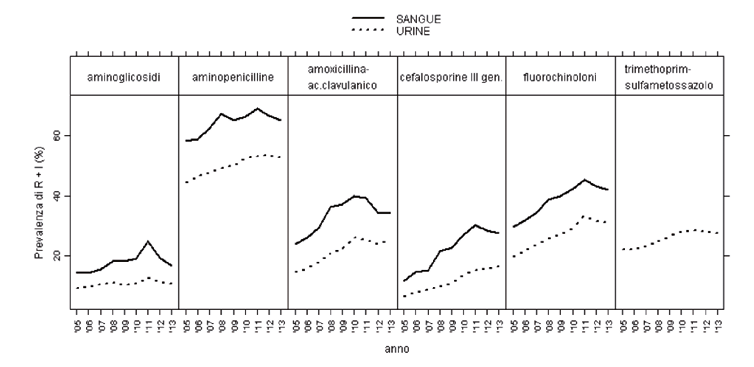 Antibioticoresistenza di Escherichia coli: emocolture/liquorcolture e urinocolture
Antibioticoresistenza di Escherichia coli: emocolture/liquorcolture e urinocoltureLa Farmacia Ospedaliera del Distretto di Scandiano ha fornito i dati di prescrizione di questi farmaci relativi sia all’ambito territoriale che a quello ospedaliero. Il quadro dell’anno 2013 mostrava un tasso di prescrizione (DDD/1000/ab./die) di FC nel distretto i Scandiano superiore alla media aziendale del 23,6%. Un’analisi più puntuale evidenziava un’abitudine prescrittiva nei quattro NCP molto differenziata, con oscillazioni tra –10,9% e +60,9 % vs. la media aziendale. La prescrizione di FC nel dipartimento di Medicina Interna dell’Ospedale di Scandiano invece era la più bassa (7,57 DDD/100 gg degenza) tra tutte le Unità Internistiche del Presidio Ospedaliero dell’AUSL, composto da cinque ospedali. In questo scenario è stato sviluppato un progetto di miglioramento della prescrizione territoriale, basato sulla ridefinizione dei criteri di appropriatezza prescrittiva dei FC, effettuata congiuntamente da MMG e da specialisti dell’Unità operativa Internistica. I Coordinatori di NCP, insieme al Responsabile del Dipartimento Internistico e al coordinatore del Comitato interaziendale controllo infezioni, hanno effettuato una revisione di letteratura e tracciato in modo volutamente sintetico gli ambiti di appropriatezza della prescrizione dei FC in ambito territoriale. Su questa base è stata elaborata una semplice scheda prospettica (vedi box) per i MMG sulla quale, all’atto della prescrizione di FC, il medico avrebbe dovuto apporre una crocetta a fianco della motivazione.
| Infezioni delle basse vie respiratorie: levofloxacina e moxifloxacina |
|
Nella polmonite in paziente
|
| Infezioni delle alte vie respiratorie: levofloxacina, moxifloxacina, prulifloxacina o ciprofloxacina |
|
| Riacutizzazione di BPCO con incremento della espettorazione o netto viraggio del catarro in paziente stadio gold 3 o 4 |
|
| Infezioni urinarie ciprofloxacina o norfloxacina |
|
In paziente
|
| Pazienti dimessi da strutture ospedaliere come proseguimento cure per: |
|
La finalità dichiarata di questa “scheda di appropriatezza” era quella di monitorare quantitativamente le motivazioni alla base delle prescrizioni di FC. Di fatto, però, la scheda sarebbe stata un promemoria delle indicazioni appropriate dei FC da utilizzare proprio nel momento in cui il MMG si accingeva a prescriverli. Nel mese di maggio 2014 sono stati organizzati incontri nei NCP del distretto, in occasione dei quali è stato presentato il progetto, corredato del materiale elaborato e dell’elenco delle prescrizioni di FC effettuate da ciascun MMG nel periodo giugno - novembre 2013. Ad ogni professionista è stato richiesto di ricostruire a posteriori la motivazione della prescrizione: R (affezioni respiratorie), U (affezioni delle vie urinarie), A (altre affezioni). Nel corso del periodo giugno – novembre 2014, durante il quale si è sviluppato il progetto, i NCP si sono incontrati due volte per discutere le criticità relative alla prescrizione e per l’analisi dei risultati parziali forniti dalla Farmacia distrettuale. Questa ha infine elaborato i dati di prescrizione di FC dei MMG del distretto nel periodo giugno - novembre 2014, confrontandoli con quelle dello stesso periodo 2013. Ha inoltre elaborato i dati relativi alla ricostruzione retrospettiva delle motivazioni alla base delle prescrizioni del periodo 2013 considerato.
Risultati
L’analisi delle motivazioni delle prescrizioni giugno-novembre 2013 ha mostrato che la causa della prescrizione era costituita dal trattamento di infezioni così ripartite:
• 55% infezioni delle vie urinarie (a loro volta ripartite 54% donne, 46% uomini);
• 30% infezioni respiratorie;
• 15% altre infezioni.
Al termine del progetto, la Farmacia distrettuale ha elaborato nuovamente i dati di prescrizione, analizzando il numero di casi (cioè di soggetti, e non di ricette) trattati dai MMG del Distretto di Scandiano.I risultati hanno evidenziato, nel periodo 2013-2014 considerato, una riduzione del numero dei casi trattati con FC pari ben al 41,5%, valore di gran lunga superiore ad ogni più ottimistica aspettativa dei partecipanti al progetto e ad altre esperienze di antibiotic stewardship in ambito territoriale.
Ulteriori variazioni nel numero dei casi trattati 2014 vs. 2013 sono state le seguenti:
• fosfomicina: +26,3%
• cefalosporine orali: +12,8%
• cotrimoxazolo: +32,7%
• trattamento con qualunque antibiotico: -6,9%.
Questa esperienza, come visto positiva, descrive il monitoraggio di un capitolo tutto sommato modesto nell’universo della prescrizione farmacologica e che ha portato ad un risultato relativamente minore rispetto a molti altri in termini di implicazioni di salute pubblica, di costi e di impatto epidemiologico. Tuttavia, il progetto può essere assunto a nostro avviso come paradigmatico di un’azione moderna di governo clinico integrata tra professionisti del territorio, specialisti ospedalieri, Servizi Farmaceutici e Direzioni aziendali. Riteniamo che vi siano alcuni punti di significato più generale che giustificano la sottolineatura di un risultato:
1. La razionalizzazione della gestione di un problema non è stata assunta come obiettivo in una logica di controllo, ma a seguito del riconoscimento del bisogno di condividere una responsabilità tra professionisti sanitari, in tutti i loro diversi ruoli.
2. Il percorso che porta alla formulazione di un quadro di riferimento – con le linee-guida che ciò comporta - non si è tradotto semplicemente in raccomandazioni affidate all’obbedienza e/o alle buone volontà dei singoli. È diventato invece il primo passo nell’adozione di un protocollo operativo che ha, nella sua necessaria semplicità, tutte le caratteristiche di un protocollo di ricerca e di sperimentazione: con le proprie regole metodologiche, gli end-point, i tempi di verifica, l’articolazione delle analisi con la restituzione e il riconoscimento dei risultati direttamente ai produttori del miglioramento.
3. La realtà quotidiana della Medicina Generale, con i suoi tempi costretti e la sua inevitabile, e spesso dichiarata ingestibile, dispersione di interessi, è stata riconosciuta come settore prioritario e possibile, per applicare e verificare interventi che molto più frequentemente vengono proposti, per lo più con strategie top-down, a livello ospedaliero.
4. Il quadro culturale che ha suggerito e definito i criteri operativi dell’esperienza è stato quello che ci ha spinto a spostare l’attenzione dal capitolo consumi (anche se gli strumenti di misura li evocano, per lo meno con riferimento alle DDD), alla visibilità e sottolineatura delle decisioni prescrittive.
In altre parole, abbiamo cercato di recuperare la coincidenza tra linee guida da una parte e persone-problemi dall’altra, riconoscendo il ruolo del clinico prescrittore come protagonista, e non come mero esecutore di politiche calate dall’alto.
Conclusioni
È stato molto chiaro per coloro che hanno partecipato all’esperienza, nei loro diversi ruoli, che la significatività statistica dei risultati, che esprime una misura quantitativa della positività dell’esperienza, può e deve diventare per la Medicina Generale significatività assistenziale e misura dell’appropriatezza culturale complessiva.
Ciò può avvenire se si innescano processi virtuosi, come riteniamo sia quello illustrato, che riconoscono responsabilità progettuali e competenze a tutti gli attori coinvolti nel progetto di cura.
Bibliografia
1. World Health Organization (WHO). Antibiotic resistance sweeping developing world. Nature 509,141–2 (08 May 2014).
2. Bax R, Green S. Antibiotics: the changing regulatory and pharmaceutical industry paradigm. J Antimicrob Chemother 2015 Jan 28. pii: dku572.
3. Borde JP, et al. Implementing an intensified antibiotic stewardship programme targeting cephalosporin and fluoroquinolone use in a 200-bed community hospital in Germany. Infection (2015) 43:45–50.
4. Davey P, et al. Interventions to improve antibiotic prescribing practices for hospital inpatients. Cochrane Database Syst Rev 2013 Apr 30; 4.
5. Davey P, et al. Time for action - Improving the design and reporting of behaviour change interventions for antimicrobial stewardship in hospitals: Early findings from a systematic review. Int J Antimicrob Agents 2015 Jan 7. pii: S0924-8579(14).
6. Arnold SR, Straus SE. Interventions to improve antibiotic prescribing practices in ambulatory care. Cochrane Database Syst Rev 2005 Oct19;(4).
7. Hamilton KW, et al. (for the CDC Prevention Epicenters Program). Point-of-Prescription Interventions to Improve Antimicrobial Stewardship. Clin Infect Dis 2015 Jan 16.
8. Leoni O, et al. La prescrizione indotta in medicina generale: il modello di analisi dell’ASL di Varese. http://www.arca.regione.lombardia.it/shared/ccurl/ 380/513/PIMG_articolo_RL.pd.
9. Robertson J et al. The impact of specialists on prescribing by general practitioners. Med J Aust 2001; 175:407-11.
10. Lim CJ, et al. Reducing inappropriate antibiotic prescribing in the residential care setting: current perspectives. Clin Interv Aging 2014; 13;9:165-77.
11. Rhee SM, Stone ND. Antimicrobial stewardship in long-term care facilities. Infect Dis Clin North Am 2014 Jun; 28(2):237-46.
12. Dyar OJ, et al. Strategies and challenges of antimicrobial stewardship in long-term care facilities. Clin Microbiol Infect 2015 Jan; 21(1):10-19.
13. Rubin MA, et al. A multifaceted intervention to improve antimicrobial prescribing for upper respiratory tract infections in a small rural community. Clin Infect Dis 2005 Feb 15; 40(4):546-53.
14. Dollman WB, et al. A community-based intervention to reduce antibiotic use for upper respiratory tract infections in regional South Australia. Med J Aust 2005 Jun 20; 182(12):617-20.
15. Little P, et al. Delayed antibiotic prescribing strategies for respiratory tract infections in primary care: pragmatic, factorial, randomised controlled trial. BMJ 2014; 348:g1606.
16. Formoso G, et al. Feasibility and effectiveness of a low cost campaign on antibiotic prescribing in Italy: community level, controlled, non-randomised trial. BMJ 2013; 347:f5391.
17. Hooton TM. Fluoroquinolones and resistance in the treatment of uncomplicated urinary tract infection. Int J Antimicrob Agents 2003 Oct; 22 Suppl 2:65-72.
18. Gagliotti C. et al. Sorveglianza dell’antibioticoresistenza e uso di antibiotici sistemici in Emilia-Romagna. Rapporto 2013. Agenzia sanitaria e sociale regionale dell’Emilia-Romagna.
*
Lino Gambarelli1, Nearco Corti2, Mirto Braglia2, Roberto Fantuzzi2, Onorato Ferrari2, Giuseppe Chesi3, Rita Montanari4, Annamaria Panciroli4, Elisa Beneventi4, Pietro Ragni5, Eletta Bellocchio6.
1 Medico di medicina generale, Direttore Dipartimento Cure Primarie Distretto di Scandiano
2 Medico di medicina generale, Coordinatore di Nucleo di Cure Primarie
3 Direttore Dipartimento Internistico Area Sud, AUSL di Reggio Emilia
4 Dipartimento Farmaceutico AUSL Reggio Emilia, Distretto di Scandiano
5 Coordinatore Comitato interaziendale Controllo infezioni AUSL di Reggio Emilia
6 Direttore Programma Cure Primarie, AUSL di Reggio Emilia