
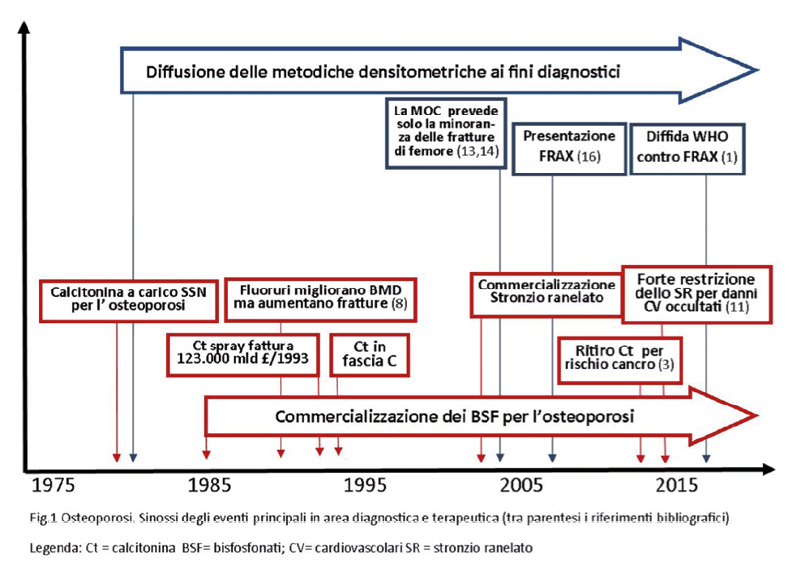
 nel 2012 quando, nel tentativo di resuscitarne l'impiego con studi clinici più consistenti, è emerso un incremento del rischio di diverse neoplasie: sia EMA che FDA hanno decretato il ritiro dal commercio degli spray nasali relegando le formulazioni iniettabili nella terapia per brevi periodi della malattia di Paget o dell'ipercalcemia grave neoplastica3.
nel 2012 quando, nel tentativo di resuscitarne l'impiego con studi clinici più consistenti, è emerso un incremento del rischio di diverse neoplasie: sia EMA che FDA hanno decretato il ritiro dal commercio degli spray nasali relegando le formulazioni iniettabili nella terapia per brevi periodi della malattia di Paget o dell'ipercalcemia grave neoplastica3.