Introduzione
La MP è la seconda più comune malattia neurodegenerativa al mondo1 e la sua prevalenza risulta in costante aumento in relazione alle modificazioni socio-demografiche della popolazione2. Infatti la prevalenza della MP aumenta costantemente con l’invecchiamento, passando da 41 casi per 100.000 abitanti nei soggetti tra 40 e 50 anni sino a raggiungere i 1900 casi per 100.000 negli ultraottantenni, con una maggiore incidenza negli anziani residenti nei Paesi sviluppati3. In Italia i pazienti affetti da Parkinson sono stimati essere 220.000, con una predilezione per il sesso maschile e con un tasso di incidenza notevolmente maggiore oltre i 70 anni di età4. Pur essendo raramente causa primaria di decesso5, i pazienti affetti da MP risultano avere una aspettativa di vita inferiore6, con un tasso di mortalità maggiore negli ultra75enni7, soprattutto a causa delle frequenti complicanze infettive polmonari8 e alla maggiore frequenza di cadute accidentali9-10. La storia naturale del MP è quella però di malattia cronica di lunga durata che porta ad una progressiva disabilità ed a perdita di autonomia, caratterizzata nelle sue fasi e tra i diversi individui da una alta variabilità clinica. La grande disomogeneità dei bisogni assistenziali della popolazione affetta da Parkinson, la frequente concomitante presenza di comorbilità rendono l’assistenza ai pazienti affetti da MP una priorità per la pianificazione socio-sanitaria in virtù dei rilevanti costi economici e sociali per il paziente e la sua famiglia. Appare pertanto indispensabile stratificare il profilo clinico della popolazione affetta da MP, riuscendo a individuare i pazienti in condizioni di terminalità o comunque con necessità di una maggiore intensità di cure, ricostruendone profilo epidemiologico, percorsi assistenziali e fattori prognostici utili nella predizione di outcome clinici. La ricerca di queste finalità richiede l’analisi di popolazioni “reali”, seguite nella loro assistenza quotidiana e non in setting precostituiti in studi clinici caratterizzati da una selezione della popolazione in studio. I DBA, attraverso l’uso di procedure e metodiche già sviluppate e validate all’interno di un programma di Health Technology Assessment che ha permesso di produrre risultati in diversi ambiti clinici11-15, assicurano, in quanto routinariamente prodotti dai sistemi sanitari, quella copertura spazio-temporale indispensabile per fornire un inquadramento di epidemiologia valutativa–assistenziale ai problemi clinico–terapeutici di una malattia come la MP.
Obiettivi
L’applicazione delle metodiche e procedure di Health Tecnology Assessment dei database amministrativi è stata declinata per definire il profilo epidemiologico-assistenziale nella popolazione pugliese dei pazienti affetti da MP inquadrandone:
1. dimensione quali-quantitiva dei soggetti affetti con particolare riferimento alla popolazione terminale/non autosufficiente;
2. identificazione dei fattori clinici (complicanze, comorbilità, durata di malattia, necessità di riabilitazione) che entrano nella definizione di gravità/gravosità assistenziale e valutazione del loro impatto sulle modalità/intensità di cure;
3. descrizione del management terapeutico attraverso l’analisi della terapia farmacologica seguita negli anni di follow-up dai pazienti nonché del ricorso a procedure terapeutiche invasive (quali la deep brain stimulation);
4. identificazione delle criticità ed aree di incertezza in relazione a bisogni inevasi/rischio di complicanze/decesso;
5. prima quantificazione dei costi sanitari diretti per ospedalizzazione e farmaci.
Materiali e metodi
L’analisi ha previsto l’utilizzo di procedure di record-linkage dei seguenti DBA:
• Schede di dimissione Ospedaliera (SDO), regionali con integrazione della mobilità passiva (anni dal 2002 al 2011);
• Prescrizioni farmaceutiche territoriali (PFT) (anni dal 2002 al 2011);
• Esenzioni per patologia (anni dal 2002 al 2011);
• Anagrafe Assistiti Regionale con integrazione delle cancellazioni per decesso/trasferimento (anni dal 2002 al 2011).
Sono stati individuati i residenti pugliesi presenti nell’anagrafe assistiti regionale almeno per un giorno nel periodo dal 01/01/2002 al 31/12/2010, quindi per l’individuazione dei pazienti affetti da MP sono stati utilizzati i seguenti criteri di inclusione:
• presenza di codice ICD9-CM 332.0 (malattia di Parkinson idiopatica, primaria) nelle SDO;
• codice 038 (morbo di Parkinson) di esenzione per patologia;
e come criterio di esclusione:
• presenza di codice 332.1 (parkinsonismo secondario) nelle SDO.
La data dell’inizio dell’esenzione o del primo ricovero con diagnosi di MP è stata considerata la data indice. La possibilità inoltre di attribuire a ciascuno dei soggetti con MP residente nella regione Puglia tutte le prescrizioni farmaceutiche (Tabella 1) dell’intero periodo esaminato (2002-2011) ha permesso di ricostruire la storia terapeutica dei singoli pazienti sia per il trattamento specifico della malattia che per ogni altra patologia e/o problema precedente, concomitante o successivo alla diagnosi di MP.
Analogamente l’attribuzione a ciascuno dei soggetti con MP della nostra coorte di tutti i propri episodi di ricovero nonché delle PFT ha consentito di valutare (in termini di rischio di decesso e, quindi, di maggiore gravità clinica) il rilevante ed indiscutibile impatto di comorbilità (valutate attraverso l’applicazione dell’indice di comorbilità di Charlson16 e dell’indice di esposizione a politerapie, DDCI15), progressione di malattia, presenza di complicanze o procedure chirurgiche invasive (Tabella 2) su specifici outcome quali 1) decesso, 2) ospedalizzazione, 3) ri-ospedalizzazione precoce, 4) costi sanitari diretti.
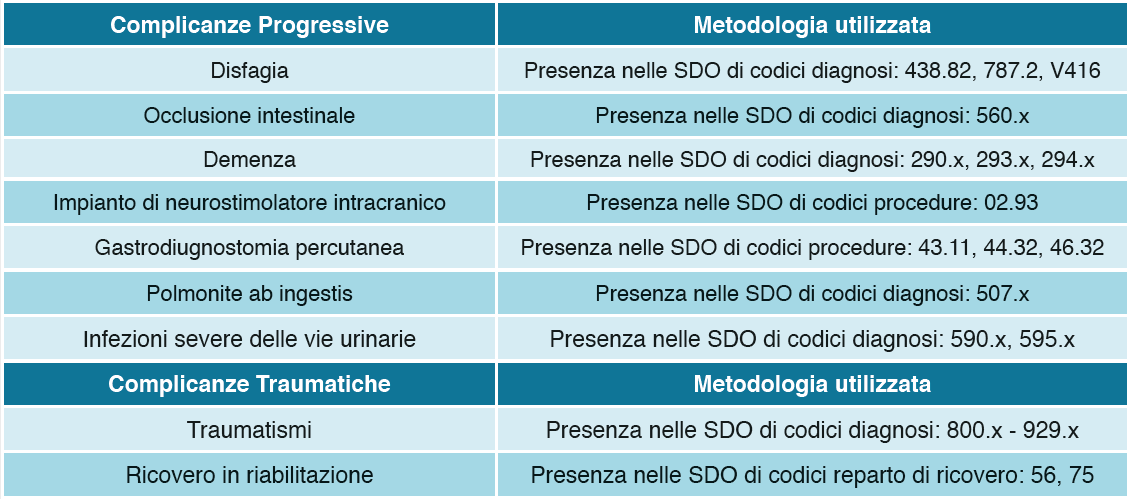 Tabella 2. Metodi e codici utilizzati per l'individuazione di complicanze/terapia invasive di supporto
Tabella 2. Metodi e codici utilizzati per l'individuazione di complicanze/terapia invasive di supporto
Risultati
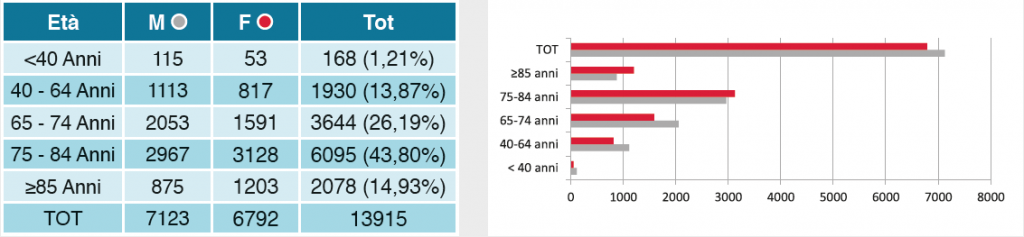
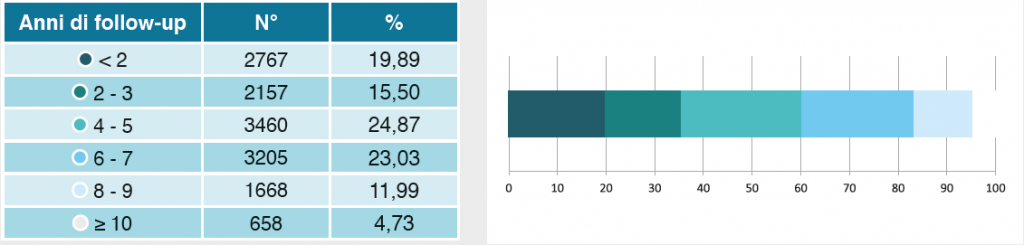
Complessivamente sono stati individuati 13.915 soggetti affetti da malattia di Parkinson idiopatico primario; la distribuzione per sesso ed età alla data di diagnosi mostra una maggiore prevalenza nel sesso maschile nelle fasce di età più giovanili, tendenza che si inverte oltre i 75 anni, fascia d’età in cui si registra la maggior parte dei casi (Figura 1a). La nostra coorte di pazienti, ricostruita su base ‘storica’, ha individuato tutti i nuovi casi di MP dal 2002 al 2010 consentendo, perciò, di ottenere dei follow-up da 1 a circa 10 anni come mostrato in Figura 1b.
Figura1. Caratteristiche dei 13.915 residenti pugliesi con diagnosi di MP nel periodo 2002-2010.
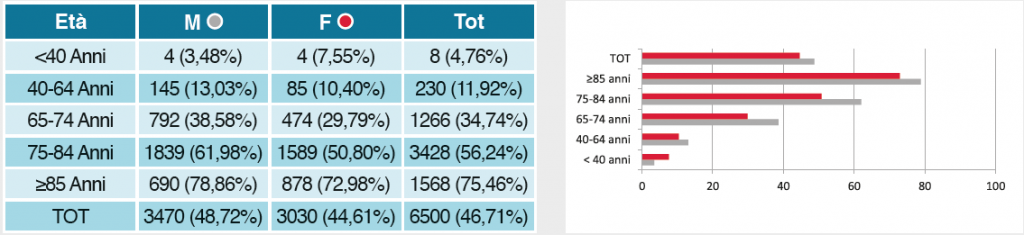
Come si evidenzia dai dati in Figura 1c, i pazienti affetti da MP costituiscono una popolazione complessa/fragile gravata da alta mortalità, soprattutto in età geriatrica, relazionabile alla frequentepresenza di complicanze/terapie invasive di supporto relazionabili al Parkinson (Tabella 3). Inoltre la maggioranza dei pazienti considerati nella nostra coorte è anziana o molto anziana e il peso delle poli-patologie associate è un elemento rilevante e non trascurabile. L’utilizzo intensivo e congiunto di più fonti amministrative di dati ha permesso di utilizzare approcci integrati di strumenti di standardizzazione della comorbilità applicabili nei diversi database:
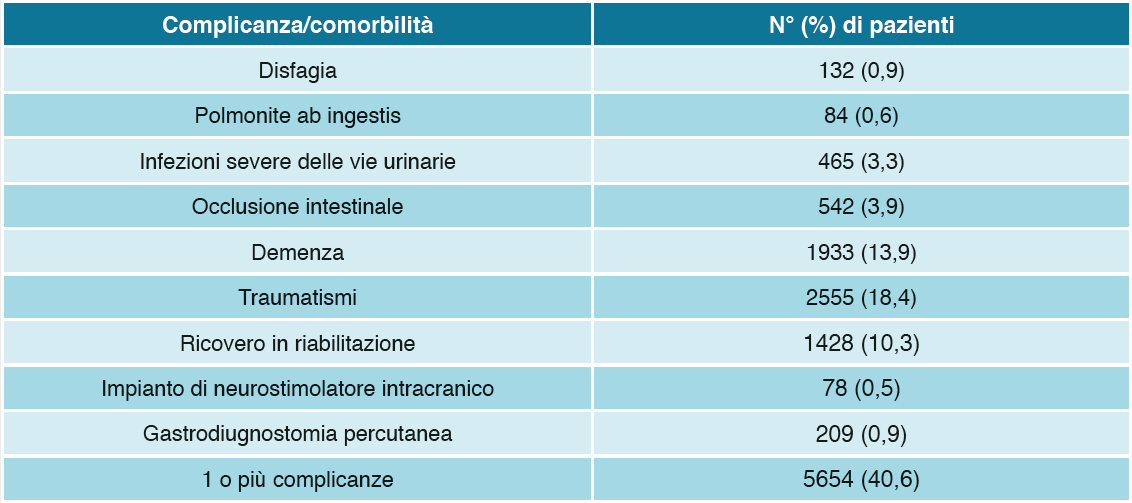 Tabella 3. Prevalenza dei pazienti con complicanze/terapie invasive di supporto relazionabili al MP
Tabella 3. Prevalenza dei pazienti con complicanze/terapie invasive di supporto relazionabili al MP
1. nelle SDO è stato applicato l’indice di comorbilità di Charlson con procedura già più volte validata/utilizzata nella letteratura internazionale16-18;
2. nelle PFT è stata valutata l’esposizione a farmaci e pattern prescrittivi diversi dal Parkinson, valutando 24 pattern prescrittivi indicativi di patologie croniche e/o problemi di salute frequenti in età avanzata ‘pesati’ attraverso un indice sintetico di complessità derivata dalla esposizione ai farmaci (DDCI)15.
Inoltre la possibilità di utilizzare l’archivio completo e storico delle PFT ha permesso di analizzare l’esposizione ai farmaci antiparkinsoniani, riportando i 5 pattern terapeutici più utilizzati come prima terapia farmacologica e mettendoli in relazione con le caratteristiche clinico-demografiche della popolazione pugliese affetta da MP (Tabella 4).
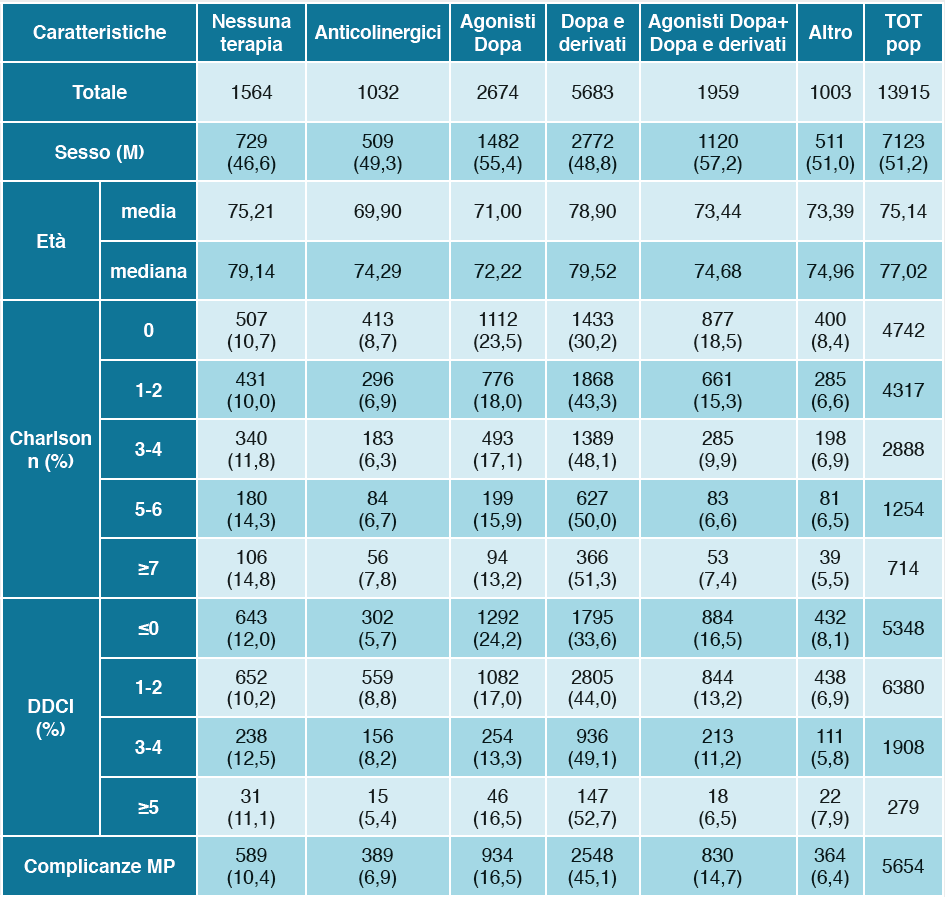
Come si può osservare dalla Tabella 4 ben 1564 (11,2%) soggetti affetti da MP non sono stati mai esposti a farmaci antiparkinsoniani. Questa coorte è risultata essere quella con la maggiore età alla diagnosi e/o con caratteristiche cliniche/comorbilità (pesate dall’Indice di Comorbilità di Charlson) più gravose.
Al contrario farmaci agonisti della Dopa ed anticolinergici sono prescritti come prima terapia nei soggetti di età inferiore e con più basso Indice di Comorbilità di Charlson, mentre pazienti con comorbilità maggiori sono preferibilmente trattati con Dopa e derivati in monoterapia.
Analogamente a quanto appena esposto per l’Indice di Comorbilità di Charlson, stratificando la nostra coorte di pazienti per DDCI o in relazione alle complicanze specifiche del MP, si conferma in modo ancora più significativo l’associazione e la tendenza all’uso di agonisti-dopa nei pazienti a bassa complessità clinica e di sola Dopa e derivati nei pazienti progressivamente più complessi.
Inoltre è stato possibile ricostruire il percorso terapeutico della popolazione con MP, analizzando le modifiche della terapia farmacologica occorse lungo il periodo di follow-up nonché il ricorso a procedure terapeutiche invasive quali la PEG o la presenza di stimolazione intracranica (Tabella 5).
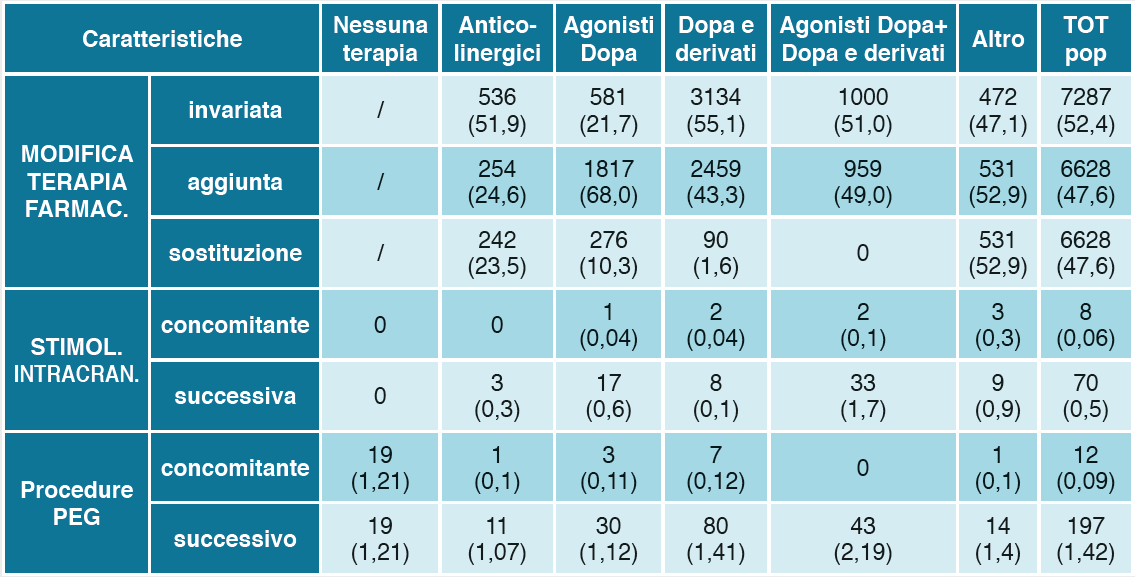 Tabella 5.Descrizione delle caratteristiche del campione di N°13.915 soggetti con MP e ' Prima terapia farmacologica' prescritta
Tabella 5.Descrizione delle caratteristiche del campione di N°13.915 soggetti con MP e ' Prima terapia farmacologica' prescritta
Si può notare come circa il 50% dei pazienti ha modificato la terapia e ciò è avvenuto indifferentemente dal farmaco iniziale; ciò che differenzia il management terapeutico è la scelta frequente di sostituire il farmaco nei pazienti che presentano come farmaci iniziali gli anticolinergici, mentre nella quasi totalità dei pazienti in terapia con Dopa e derivati vi è la decisione di aggiungere un farmaco ulteriore. Procedure terapeutiche invasive (quali la stimolazione intracranica e la PEG) risultano essere scelte terapeutiche successive/alternative al fallimento della terapia farmacologica nei pazienti “limite” al alto grado di complessità/criticità. Bisogna inoltre sottolineare come tra gli altri farmaci, vi sia il frequente ricorso all’Entacapone come farmaco di seconda linea: presente nel 33% dei soggetti che hanno subito modificazioni della terapia. In ultimo è stato analizzato l’impatto di comorbilità, complicanze progressive o accidentali e della difficoltà nel management farmaceutico dei pazienti affetti da MP (valutata attraverso il ricorso a politerapie complesse) su end-point clinici (quali il rischio di decesso e di ospedalizzazione) nonché su costi/indicatori di gravosità assistenziale (Tabella 6-7-8).
Procedure terapeutiche invasive (quali la stimolazione intracranica e la PEG) risultano essere scelte terapeutiche successive/alternative al fallimento della terapia farmacologica nei pazienti “limite” al alto grado di complessità/criticità. Bisogna inoltre sottolineare come tra gli altri farmaci, vi sia il frequente ricorso all’Entacapone come farmaco di seconda linea: presente nel 33% dei soggetti che hanno subito modificazioni della terapia. In ultimo è stato analizzato l’impatto di comorbilità, complicanze progressive o accidentali e della difficoltà nel management farmaceutico dei pazienti affetti da MP (valutata attraverso il ricorso a politerapie complesse) su end-point clinici (quali il rischio di decesso e di ospedalizzazione) nonché su costi/indicatori di gravosità assistenziale (Tabella 6-7-8).
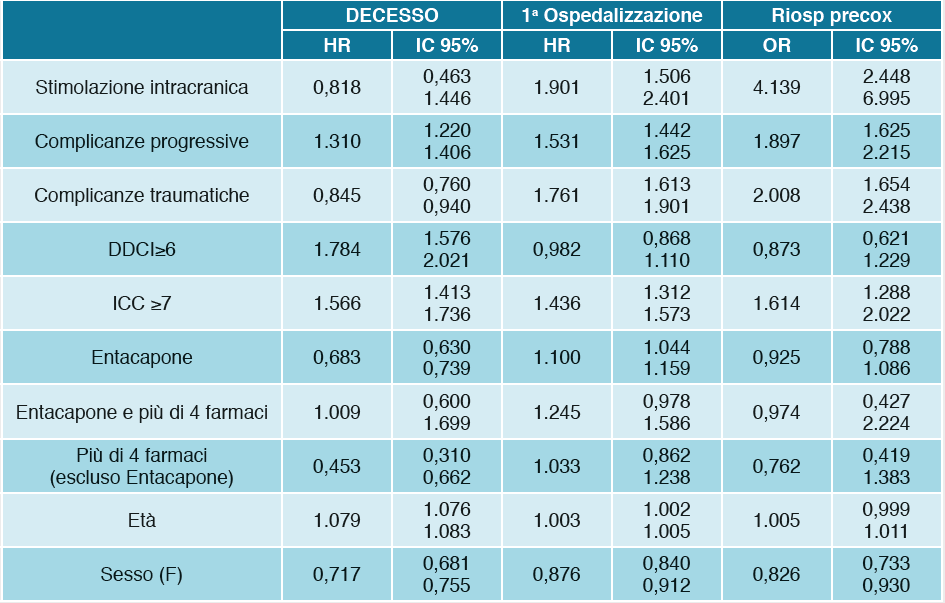
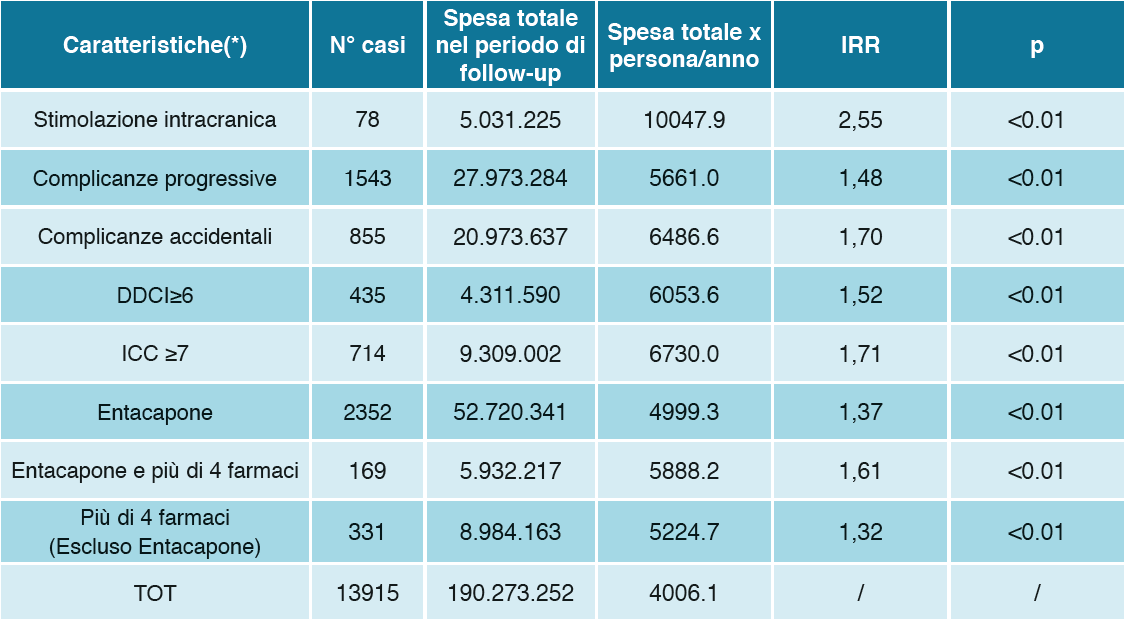 Tabella 7. Spesa Totale e per persona/anno per caratteristiche cliniche dei pazienti affetti da MP (*)
Tabella 7. Spesa Totale e per persona/anno per caratteristiche cliniche dei pazienti affetti da MP (*)
Discussione
L’uso di più fonti di dati amministrativi, quali quelle qui utilizzate, se limitanti dal punto di vista clinico-specialistico (assenza di conferma diagnostica, di esordio di malattia e di scale di gravità) risultano invece molto ricche di contenuto informativo nella valutazione più complessiva e globale delle condizioni di salute/malattia di ampie popolazioni di assistiti in condizioni di ‘normale pratica clinica quotidiana. L’attendibilità dei risultati ottenuti dall’utilizzo intensivo dei dati amministrativi trova conferma dalla sovrapponibilità dei dati di prevalenza con quelli enunciati dai centri epidemiologici nazionali4, attestandosi a circa 350 casi ogni 100.000 abitanti. L’utilizzo di dati correnti relativi all’assistenza “usuale” attuata nei pazienti affetti da MP ha permesso di analizzarne percorsi terapeutici reali, permettendo di analizzare le prime terapie prescritte, nonché eventuali modalità di modifica delle stesse. In tal senso appare interessante sottolineare come l’uso di monoterapia, come prima terapia farmacologica, era presente nel 67,5% dei pazienti, più precisamente, con Dopa e derivati nel 40,8%, con agonisti-dopa nel 19,2% e con anticolinergici nel 7,5% dei soggetti con MP primitiva.
È da sottolineare inoltre come 11,2% dei pazienti non risultavano esposta ad alcuna terapia specifica, dato questo che testimonia/conferma la bassa compliance terapeutica che caratterizza la popolazione affetta da MP19. Appare inoltre rilevante la percentuale di soggetti che presenta già alla diagnosi una terapia specifica con almeno 2 classi farmaceutiche differenti, assommando una popolazione pari al 21,3% del campione totale e testimoniando, congiuntamente all’alta prevalenza di soggetti che modificano la terapia nel corso del follow-up, la difficoltà gestionale di questa patologia che espone i pazienti a switch terapeutici in quasi il 50% dei casi20.
Le modifiche terapeutiche mostrano come vi sia un concomitante incremento dei soggetti esposti a politerapie più o meno complesse e il ricorso ad associazioni con Entacapone, che risulta il farmaco più utilizzato in seconda linea. Si è potuto inoltre mettere in luce come vi siano categorie di farmaci quali gli agonisti della Dopa e gli anticolinergici utilizzati in popolazioni più giovani o comunque a minor rischio clinico, mentre come terapia per soggetti gravati da comorbilità (misurata attraverso il Charlson) o ad alta complessità di cure (valutata attraverso il DDCI) viene preferito l’utilizzo di Dopa e derivati. La popolazione affetta da MP è risultata essere ad alta gravità clinica presentando un tasso di mortalità molto elevato e alti punteggi negli strumenti di stratificazione del rischio clinico; infatti i sopravvissuti alla fine del periodo di follow-up sono stati il 53,3% e una alta percentuale di pazienti è stata gravata dalle complicanze specifiche del MP, influendo negativamente sulla indipendenza e qualità di vita21.
La definizione delle caratteristiche clinico-demografiche della popolazione pugliese affetta da MP e la valutazione del loro impatto su end-point population-based quali decesso, ospedalizzazione, riospedalizzazione precoce e costi sanitari diretti, ha permesso di poter stratificare il profilo di rischio clinico di ogni paziente in relazione alle caratteristiche specifiche della gravità del quadro di MP nonché delle comorbilità/complessità ad esso associato. Infatti l’età avanzata, il sesso maschile, un punteggio all’indice di Comorbilità di Charlson maggiore di 6 e al DDCI maggiore di 5 e la presenza di complicanze specifiche del MP sono risultati come fattori strettamente associati al peggioramento di tutti gli outcome clinici ed assistenziali esaminati.
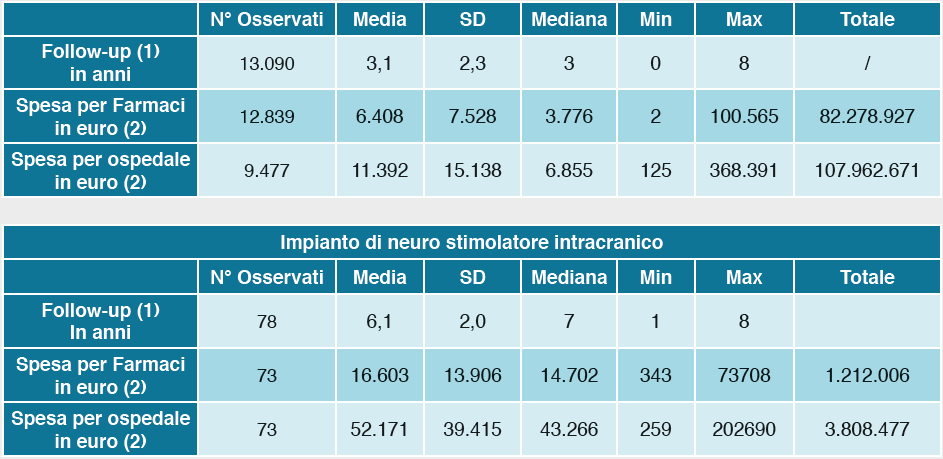
La presenza invece di impianto di neuro stimolatore intracranico, in 78 soggetti della nostra coorte, era associato a più basso rischio di decesso (probabilmente in relazione alla selezione di pazienti in migliori condizioni cliniche e di più giovane età) ma a maggiore frequenza di ospedalizzazione, ri-ospedalizzazione e più elevati costi sanitari diretti (valutati sia come spesa complessiva che come spesa/persona/anno). Analogamente l’utilizzo dei database amministrativi nella conoscenza-definizione dei diversi livelli di gravità-disabilità può risultare utile nella identificazione di sottopopolazioni ad alto rischio eventualmente candidabili a trattamenti intensivi utili a ridurre complicanze ed ospedalizzazioni come ad esempio nel caso della terapia per uso infusionale intra duodenale di levodopa e carbidopa.
L’utilizzo integrato di sorgenti dati amministrative di popolazioni altamente rappresentative da un punto di vista quali-quantitativo può fornire la base conoscitiva per la coniugazione con una strategia mirata a raccogliere prospetticamente, con un sistema informatico adottabile da reti di centri clinici, dati ad hoc che permettano di qualificare in modo più completo le storie cliniche e terapeutiche dei pazienti portatori delle patologie indice, e di sviluppare reti operative interessate ed in grado di gestire programmi di monitoraggio prospettico delle stesse patologie e relative terapie, nonché nella valutazione e definizione dei costi sociali, del coinvolgimento di famiglia e caregivers e delle perdita di produttività ed autonomia.
Conclusioni
La costruzione di un data set integrato di dati ricavati da diversi flussi informativi con completa copertura territoriale (e di popolazione) e ampia copertura temporale si conferma come risorsa rilevante ed inesauribile di analisi, valutazioni e ricerca in ambito epidemiologico con una attenzione particolare ai contesti assistenziali di una normale pratica quotidiana. La coniugazione di questo approccio con una strategia mirata a raccogliere prospetticamente dati clinico-terapeutici ad hoc permetterebbe non solo di rispondere a quesiti epidemiologici specifici ma anche di promuovere la formazione del personale operante nelle reti nell’area della epidemiologia clinico–assistenziale e della valutazione economico–gestionale dei relativi percorsi assistenziali attraverso la strutturazione di reti integrate tra strutture amministrative e centri clinici.
1. de Lau LM, Breteler MM. Epidemiology of Parkinson's disease. Lancet Neurol 2006 Jun; 5(6):525-35.
2. Kusumi M, Nakashima K, Harada H, et al. Epidemiology of Parkinson’s disease in Yonago City, Japan: Comparison with a study carried out 12 years ago. Neuroepidemiology 1996; 15:201-207.
3. Pringsheim T, Jette N, Frolkis A, Steeves TD. The prevalence of Parkinson's disease: A systematic review and meta-analysis. Mov Disord 2014 Jun 28.
4. Istituto Superiore di Sanità. Available on: http://www.epicentro.iss.it.
5. Phillips NJ, Reay J, Martyn CN. Validity of mortality data for Parkinson’s disease. J Epidemiol Community Health 1999; 53:587-588.
6. Tanner CM, Thelen JA, Offord KP, et al. Relationship of age at diagnosis to survival in Parkinson’s disease. Mov Disord 1992; 7:104.
7. Lilienfeld DE, Chan E, Ehland J, et al. Two decades of increasing mortality from Parkinson’s disease among the US elderly. Arch Neurol 1990; 47:731-734.
8. Nakashima K, Maeda M, Tabata M, et al. Prognosis of Parkinson’s disease in Japan. Eur Neurol 1997; 38:60-63.
9. Gazibara T, Pekmezovic T, Kisic Tepavcevic D, Tomic A, Stankovic I, Kostic VS, Svetel M. Fall frequency and risk factors in patients with Parkinson's disease in Belgrade, Serbia: A cross-sectional study. Geriatr Gerontol Int 2014 Apr 28.
10. Benzinger P, Rapp K, Maetzler W, König HH, Jaensch A, Klenk J, Büchele G. Risk for femoral fractures in Parkinson's disease patients with and without severe functional impairment. PLoS One 2014 May 22; 9(5):e97073.
11. De Berardis G, Lucisano G, D’Ettorre A, Pellegrini F, Lepore V, Tognoni G, Nicolucci A. Association of aspirin use with major bleeding in patients with and without diabetes. JAMA 2012; 307(21): 2286-94.
12. Monte S, Macchia A, Pellegrini F et all. Antithrombotic treatment is strongly underused despite reducing overall mortality among high-risk elderly patients hospitalized with atrial fibrillation. Eur Hearth J 2006; 27:2217-2223.
13. Monte S, Fanizza C, Romero M, Rossi E, De Rosa M, Tognoni G. Administrative databases as a basic tool for the epidemiology of cardiovascular disease. G Ital Cardiol 2006; 3:206-216.
14. De Berardis G, Robusto F, D’Ettorre A, Lepore V, Nicolucci A, Attolini E, Bisceglia L. Incidenza dei ricoveri per ipoglicemia e costi associati nelle persone con diabete mellito. Informazioni sui Farmaci 2014; 38(1):8-13.
15. Robusto F, Lepore V, Bisceglia L, Petrarolo V. Epidemiologia assistenziale della fragilità-complessità delle popolazioni anziane (Parte I). Informazioni sui Farmaci 2013; 37(1):17-23.
16. D'Hoore W, Sicotte C, Tilquin C. Risk adjustment in outcome assessment: the Charlson comorbidity index. Methods Inf Med 1993 Nov; 32(5):382-7.
17. Lix LM, Quail J, Fadahunsi O, Teare GF. Predictive performance of comorbidity measures in administrative databases for diabetes cohorts. BMC Health Serv Res 2013 Aug 17; 13:340.
18. Christensen S, Johansen MB, Christiansen CF, Jensen R, Lemeshow S. Comparison of Charlson comorbidity index with SAPS and APACHE scores for prediction of mortality following intensive care. Clin Epidemiol 2011; 3:203-11.
19. Wei YJ, Palumbo FB, Simoni-Wastila L, Shulman LM, Stuart B, Beardsley R, Brown CH. Antiparkinson drug adherence and its association with health care utilization and economic outcomes in a Medicare Part D population.Value Health 2014 Mar; 17(2):196-204.
20. Wei YJ, Palumbo FB, Simoni-Wastila L, Shulman LM, Stuart B, Beardsley R, Brown C. Antiparkinson drug use and adherence in medicare part D beneficiaries with Parkinson's disease. Clin Ther 2013 Oct; 35(10):1513-1525.
21. Hechtner MC, Vogt T, Zöllner Y, Schröder S, Sauer JB, Binder H, Singer S, Mikolajczyk R. Quality of life in Parkinson's disease patients with motor fluctuations and dyskinesias in five European countries. Parkinsonism Relat Disord 2014 Jun 10. pii: S1353-8020(14):00219-3.
Data di Redazione 8/2014
Con questo terzo contributo (vedi ISF 2013; n. 1: pag. 17-23 e ISF 2013; n. 2: pag. 38-42) prosegue il nostro percorso dentro l’universo della/e fragilità-complessità delle persone anziane e non.
Percorso che è insieme dialogo e formazione ad una Epidemiologia Assistenziale quale componente imprescindibile per una pratica responsabile della presa in carico diagnostico-preventiva-terapeutica delle popolazioni più gravose.
L’approccio metodologico è quello già descritto:
• saper riconoscere e identificare, nella "non misurabile variabilità" della pratica quotidiana, coorti di pazienti-cittadini sufficientemente omogenei per caratteristiche cliniche, socio-demografiche e/o bisogni;
• utilizzando i Database Amministrativi (DBA) che, per completezza spaziale (per esempio una intera regione) e temporale (per esempio un arco temporale di 10 anni), costituiscono una eccezionale risorsa conoscitiva per approfondimenti sempre nuovi;
• per produrre ‘rapporti’ che non si limitino a fotografare l’esistente ma più interessati (attraverso follow-up longitudinali di coorti di pazienti) ad evidenziare le storie, i percorsi e gli esiti della popolazione assistita e, in modo particolare, di 'minoranze' particolarmente a rischio e/o portatrici di gravità clinica e gravosità assistenziale sempre e inevitabilmente correlate ad un maggior consumo di risorse.
La proposizione della/e popolazione/i portatrice/i di Malattia di Parkinson (MP) della regione Puglia è un buon esempio-modello di questo risultato. Infatti la possibilità di diverse opzioni terapeutiche, la cronicità, lunga durata e progressione caratterizzata da alta disabilità nelle fasi avanzate, con costi economici e sociali elevati per il paziente e la sua famiglia, conferma la MP come scenario esemplare di fragilità/complessità.
La possibilità di qualificare definizioni e termini, oggi così diffusi e [ab]usati, verificando operativamente, su popolazioni reali, se, come, quanto e quando siano applicabili, è un ulteriore prodotto del nostro percorso di "Epidemiologia assistenziale della fragilità-complessità" già auspicato sin all’inizio di tale lavoro (vedi ISF 2013; n. 1: pag. 22).